Придатність відходів цукрових буряків для виробництва водневмісного газу

Енергетика відіграє важливу роль у формуванні та підтримці сучасної економіки. З індустріалізацією постійно зростає потреба в енергії, для задоволення якої використовуються викопні види палива, ядерне паливо та відновлювані джерела енергії. Найважливішими причинами нещодавнього зростання інтересу до альтернативних відновлюваних джерел енергії є обмеженість викопного палива, коливання цін на нафту, загрози зміни клімату та незворотна шкода навколишньому середовищу. Сьогодні технологія відновлюваної енергії визначається як велика прикладна наука, яка поступово витіснить звичайне викопне паливо.
За матерілами статті на тему «Оцінка відходів цукрових буряків у виробництві багатого водень газу» («Evaluation of Sugar Beet Waste in the Production of Hydrogen-Rich Gas») «Міжнародного журналу з досліджень відновлюваної енергетики» («International Journal of Renewable Energy Research»), вересень 2019 р.
Водень займає чільне місце у відновлюваних джерелах енергії через свої переваги, включаючи високий вихід енергії, відсутність шкідливих викидів, а також можливість його виробництва з різноманітної сировини. У зв’язку з цим останніми роками виробництво водню привертає до себе все більше уваги. Водень має величезний діапазон застосування, що варіюється від виробництва електроенергії (паливних елементів, газових турбін, децентралізованих енергетичних систем, двигунів внутрішнього згоряння, ракетних паливних систем тощо) до виробництва тепла. Більше того, однією з багатьох особливостей водню, що привертає увагу, є вищезгадана можливість його виробництва з широкого спектру ресурсів, таких як викопне паливо, невикопне паливо, біомаса та вода за допомогою різних методів, таких як електроліз, переробка палива та термохімічне розкладання води. Серед цих ресурсів і методів отримання водню з біомаси виділяються такі аспекти, як низька вартість сировини, низький рівень викидів газу сухої перегонки та можливість переробки органічних відходів.
Газифікація біомаси — це термохімічне перетворення твердих, рідких і газоподібних продуктів, включаючи CH4, H2, CO та CO2. По суті, газифікація біомаси складається з чотирьох етапів: попереднє нагрівання та сушіння, піроліз, газифікація коксового залишку та спалювання. У звичайних умовах газифікації шляхом попереднього нагрівання з біомаси видаляється волога, а при піролізі біомаса розкладається на сухі речовини, рідини та гази. На етапі піролізу утворюються коксовий залишок, смола і димові гази. Після цього утворені продукти переходять до етапу газифікації, де відбуваються реакції між коксовим залишком і газифікуючим агентом з утворенням легких цінних газів, таких як CO2 та H2. Реакція горіння має вирішальне значення для бажаної газової суміші, оскільки будь-який надмірний окислювач без потреби підвищує температуру і порушує якість газу, розбавляючи його з CO2. У процесі газифікації перетворення біомаси в газоподібні продукти з доданою вартістю тягне за собою велику кількість енергії, тому для досягнення бажаної ефективності та нижчої температури процесу використовується каталізатор. Для цього використовуються NaOH, KOH, Na2CO3, K2CO3, Ca(OH)2 та деякі каталізатори перехідних металів (Ni, Co). Крім того, обсяг коксового залишку та смоли, який неможливо зменшити до розумної кількості, створює деякі експлуатаційні та технічні проблеми, що вимагає подальшої обробки. Основні реакції, що відбуваються під час газифікації біомаси:
Біомаса → газ + смола + коксовий залишок (1)
Реакції горіння
C + 0,5O2 → CO -111 МДж/кмоль (2)
CO + 0,5O2 → CO2 -283 МДж/кмоль (3)
H2 + 0,5O2 → H2O -242 МДж/кмоль (4)
Реакція Будуа
C + CO2 →2CO +172 МДж/кмоль (5)
Водно-газова реакція
C + H2O ↔ CO + H2 +131 МДж/кмоль (6)
Реакція метанування
C + 2H2 ↔ CH4 -75 МДж/кмоль (7)
Реакція конверсії водяного газу
CO + H2O ↔ CO2 + H2 -41 МДж/кмоль (8)
Реакція парового риформінгу
CH4+ H2O → CO + 3H2 -206 МДж/кмоль (9)
Цукровий буряк складається в основному з 75% води, 20% цукру і 5% жому. Буряковий жом, побічний продукт цукрової галузі, багатий на целюлозу, геміцелюлозу, пектин, а також містить невелику частку лігніну. Жом часто використовується як джерело для кормів для тварин, але продовжуються дослідження різних способів його використання.
У літературі є низка повідомлень про газифікацію різних видів біомаси, однак досить мало досліджень щодо відходів цукрових буряків, вчені зосереджувалися на екстракції та характеристиці пектину з бурякового жому.
Тому дане дослідження спрямоване на вивчення газифікації відходів цукрових буряків для отримання газу з високим вмістом H2. Досліджено вплив температури реакції та каталізатора на розподіл та вихід газоподібного продукту, ефективність перетворення вуглецю та теплотворність. Тим більше, що лужний каталізатор, особливо K2CO3, відомий як хороший каталізатор для газифікації біомаси. Крім того, він дешевший, ніж каталізатор на основі металу (Cu/Ru), та має кращу реакційну здатність, ніж каталізатори з перехідних металів (Fe/Ni), що робить його (лужний каталізатор) привабливим для застосування в газифікації біомаси. Отже, враховуючи все вищесказане, для каталітичної газифікації відходів цукрових буряків було обрано два каталізатори K2CO3 та Na2CO3.
Результати та обговорення
Склад відходів цукрових буряків
Склад відходів цукрових буряків наведено в Таблиці 1. Усі відходи, незважаючи на різний відсотковий вміст, значною мірою містять геміцелюлозу та целюлозні компоненти. Відходи неекстрагованих цукрових буряків (WUNESB) багаті геміцелюлозою, тоді як і жом, і бадилля (гичка) буряка багаті целюлозою. Жом має найвищий вміст лігніну, а в WUNESB і бадиллі його вміст майже однаковий. Крім того, вилучений обсяг помітно змінюється залежно від типу відходів; виявляється, що жом демонструє найменшу кількість вилучених речовин, тоді як найвищий вміст речовин можна отримати з відходів неекстрагованих цукрових буряків (WUNESB). Незважаючи на відсутність суттєвих відмінностей у вмісті золи серед відходів, найбільшу частку золи має WUNESB.
Таблиця 1. Результати технічного та хімічного аналізу жому, відходів неекстрагованих цукрових буряків (WUNESB) та бурякового бадилля (гички)
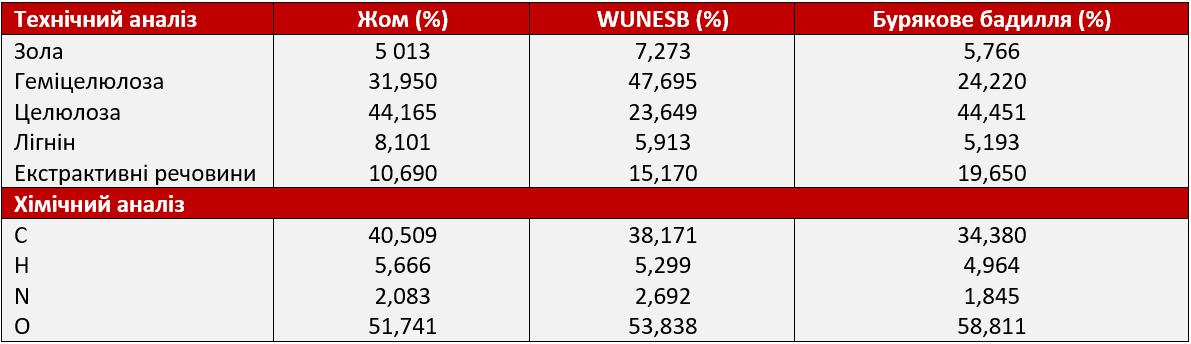
* Бензол-етанольні екстрактивні речовини.
Газифікація відходів цукрових буряків
Жом
Вплив температури: температура має важливий вплив на загальну газифікацію біомаси. Виходячи з принципу Лешательє, температурний вплив на продуцентний газ залежить від термодинамічної поведінки реакцій. Газифікація біомаси включає велику кількість екзотермічних та ендотермічних реакцій. Таким чином, контроль температури має вирішальне значення для досягнення високої якості генераторного газу, а вища температура сприяє реагентам в екзотермічних реакціях і продуктам ендотермічних реакцій.
Для визначення впливу температури реакції на вихід водню досліди проводилися в умовах ріїного температурного режиму (650, 750 і 850°С) із використанням певної кількості відходів цукрових буряків за відсутності каталізатора та 15 хв. час реакції.
Як показано на Рис. 1, температуру в газогенераторі поступово (на 100°C) збільшували з 650°C до 850°C, при цьому вихід водню постійно збільшувався. При температурі 650°C його вихід склав 3,220 моль H2/кг жому. При підвищенні температури реакції з 750 до 850°C вихід водню істотно збільшився з 4,424 до 5,730 моль H2/кг жому. Із Рис. 1 можна зробити висновок, що температура є сприятливою для збільшення виходу водню. Це може бути пов’язано з тим, що збільшення температури забезпечує відповідне середовище для ендотермічних реакцій. Отже, реакція Будуа (Рівняння 5), реакція конверсії водяного газу (Рівняння 6) і реакція парового риформінгу (Рівняння 9) стають домінуючими і відповідають в основному за утворення водню при підвищеній температурі, тоді як при вищій температурі реакція конверсії водяного газу (Рівняння 8) є злегка екзотермічною і менш важливою.
Рис. 1. Вплив температури на вихід водню, отриманого при газифікації жому (без каталізатора, швидкість подачі повітря 2 л/год, час реакції 15 хв.)
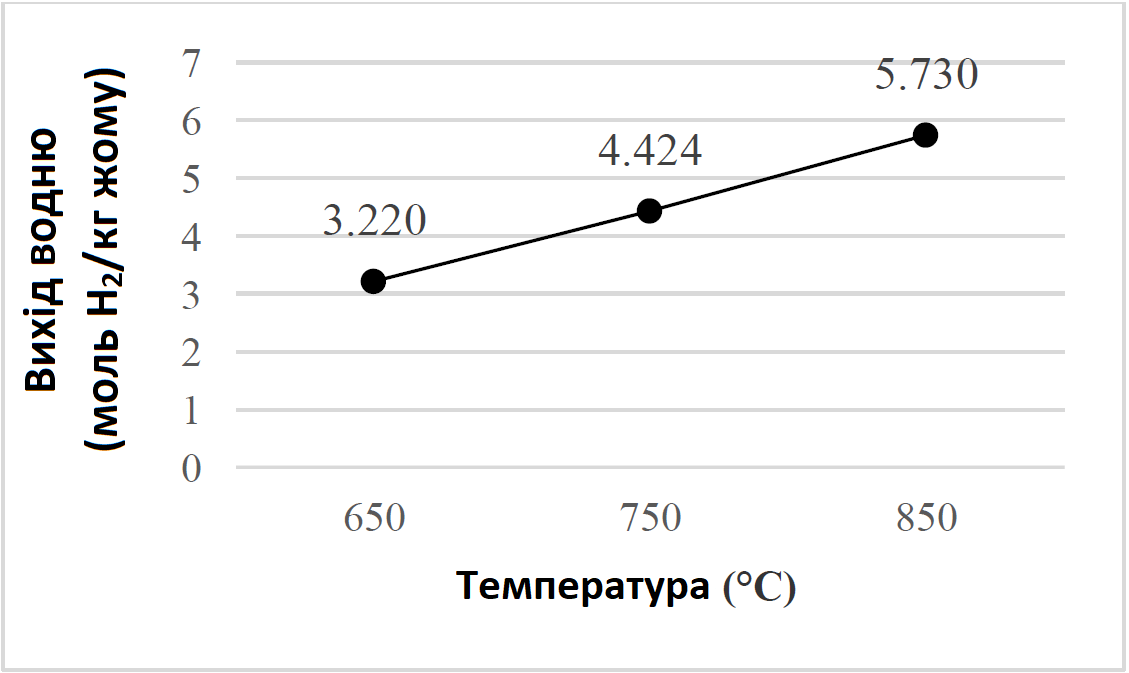
Параметри ефективності газифікації, такі як вихід газу, ефективність перетворення вуглецю та газу з низькою теплотою згоряння, аналізували за різних температурних умов. Із Таблиці 2 видно, що з підвищенням температури вихід газу, який можна охарактеризувати як частку жомових частинок, перетворених на газоподібні продукти, значно збільшується з 0,740 до 0,900 STP м3/кг жому. Це означає, що вища температура призвела до більшого перетворення жому в газоподібний продукт. Збільшення виходу газу можна пояснити спільним впливом реакцій піролізу, видалення летучих речовин, а також реакцій газифікації та підвищення температури. Тим часом при заданому діапазоні температур конверсія вуглецю також збільшилася з 84,716% до 95,061%, що підтверджує результат виходу газу, оскільки підвищення температури зробило можливим виділення більшої кількості газоподібних продуктів (Таблиця 2).
Таблиця 2. Експериментальний результат впливу різної температури газегенератора (без каталізатора, швидкість подачі повітря 2 л/год, час реакції 15 хв.)
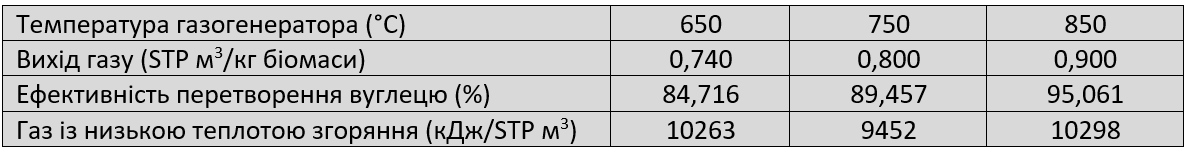
Температура має значний вплив на склад отриманого газу. Вміст H2 і CO в генераторному газі відіграє важливу роль у його подальшому використанні. Як показано на Рис. 2, вміст СО демонстрував тенденцію до збільшення з підвищенням температури. Він також перевищував вміст H2 при всіх досліджуваних температурних режимах і досягнув свого максимального значення при 850°C — 8,861 моль/кг жому. Із підвищенням температури часткове окислення коксу (Рівняння 2), реакція Будуа (Рівняння 5), а також водно-газова реакція (Рівняння 6) посилювалися, що могло зробити величезний внесок у вміст CO. CH4 було отримано за допомогою реакції метанування (Рівняння 7) та реакції парового риформінгу (Рівняння 9), що відбувалися під час газифікації біомаси. Високий вміст CH4 було отримано, коли реакція розпочалася при 650°C зі значенням 1,480 моль/кг жому, однак подальше підвищення температури майже не вплинуло (невелике зниження) на вихід CH4. Тому вища температура несприятлива для утворення СН4. Для досягнення кращої якості горючих газів під час газифікації біомаси враховується вміст CO2, оскільки він призводить до зниження теплотворності та ускладнює процеси очищення. У дослідженні підвищення температури не показало очевидних змін у виділенні CO2, за винятком експерименту, проведеного при 850°C, коли спостерігалося незначне його збільшення. Кількість етан-пропану зменшилася з 0,401 до 0,313 моль/кг жому, коли температура збільшилася з 650 до 750°C, тоді як при 850°C з подальшим підвищенням температури вміст етан-пропану демонстрував протилежну тенденцію — було виявлено 0,542 моль/кг жому. Виділялася зміна етан-пропану, оскільки як CH4, так і етан-пропан мають більшу теплотворну здатність, порівняно з іншими видами генераторного газу. Отже, газ із низькою теплотою згоряння подібним чином зменшився при 750°C, але досягнув максимального значення 10298 кДж/STP м3 при 850°C.
Рис. 2. Вплив температури на склад генераторного газу (без каталізатора, швидкість подачі повітря 2 л/год, час реакції 15 хв.)
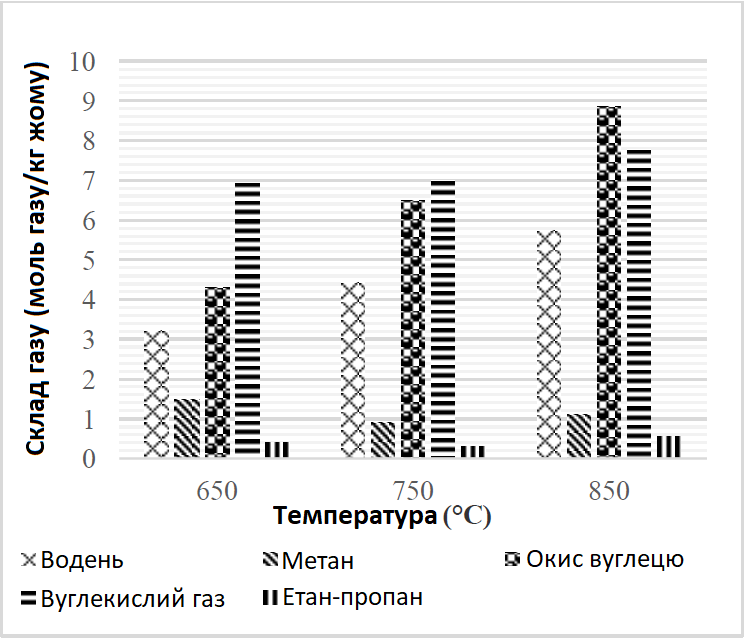
Вплив коефіцієнта каталізатора: процеси газифікації тягнуть за собою високі температури для зменшення залишків смоли і перетворення біомаси в цінний газоподібний родукт, такий як водень. Ця висока енергетична потреба погіршує економічну життєздатність процесів газифікації. Тому нижча температура газифікації є бажаною не тільки для енергоефективності, а й для запобігання експлуатаційних проблем, пов’язаних із високими температурами. Каталітична газифікація біомаси як перспективна методика дозволяє біомасі газифікуватися при більш низькій температурі, що сприяє високій конверсії та термічній ефективності. Крім того, оптимізація видалення смоли та покращення синтез-газу можуть бути досягнутими за допомогою відповідного каталізатора.
На відміну від некаталітичного дослідження, каталітичне дослідження проводилося при 650°C з вище зазначених причин. Каталізатор додавали безпосередньо до біомаси шляхом сухого змішування. У якості каталізатора використовували K2CO3, експерименти проводилися з різними співвідношеннями кількості каталізатора до кількості сировини (20%, 30%, 40%), результати яких показано на Рис. 3.
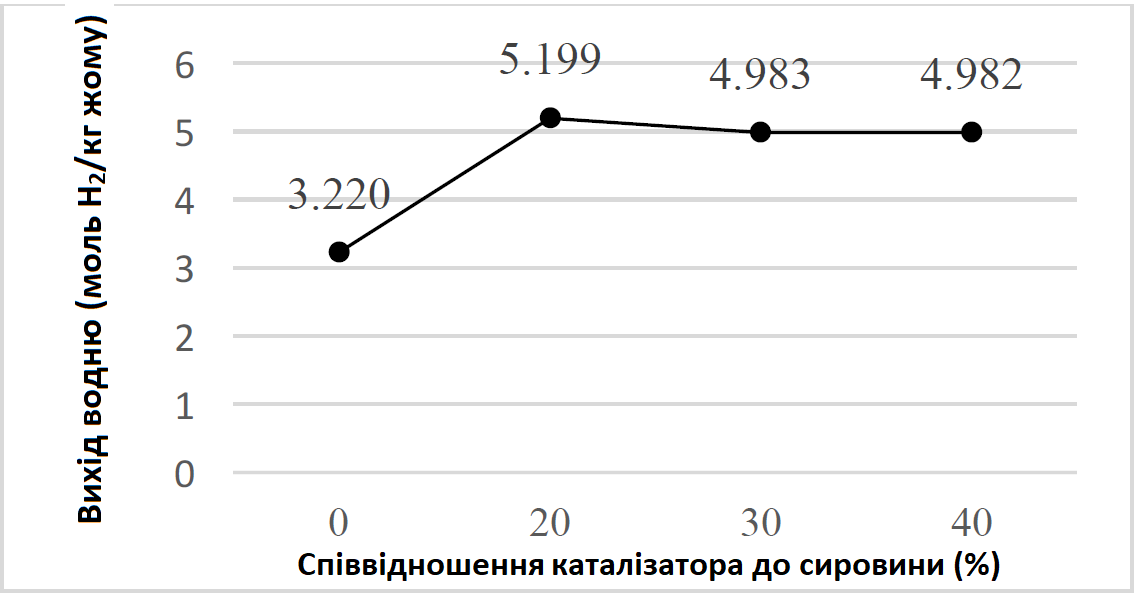
Спочатку вихід водню швидко зростав, досягнувши 20% співвідношення кількості каталізатора до кількості сировини з виходом 5,199 моль H2/кг жому. Як зазначалося раніше, можливою причиною, що пояснює це явище, є домінування реакції конверсії водяного газу при нижчій температурі у супроводі каталізатора. Після цього вихід водню дещо зменшився до 4,983 моль H2/кг жому при 30% співвідношенні кількості каталізатора до кількості сировини. Подальше додавання каталізатора, як виявилося, не викликало істотної зміни у виході водню, і він тримався на тому ж рівні. Згідно з отриманими результатами, навіть незважаючи на те, що каталізатор K2CO3 продемонстрував нижчі показники виходу водню, порівняно з дослідженням без використання каталізатора при 850°C, він все ще виявляється ефективним щодо виробництва водню при 20% співвідношенні кількості каталізатора до кількості сировини. Таким чином, дана ситуація виправдала всі очікування та дала бажаний результат, оскільки використання каталізатора допомогло знизити витрати енергії та перешкоджало експлуатаційним проблемам щодо більш високої температури.
Рис. 3. Вплив коефіцієнту співвідношення кількості каталізатора (K2CO3) до кількості сировини на вихід водню, отриманого під час газифікації жому (650°C, швидкість подачі повітря 2 л/год, час реакції 15 хв.)
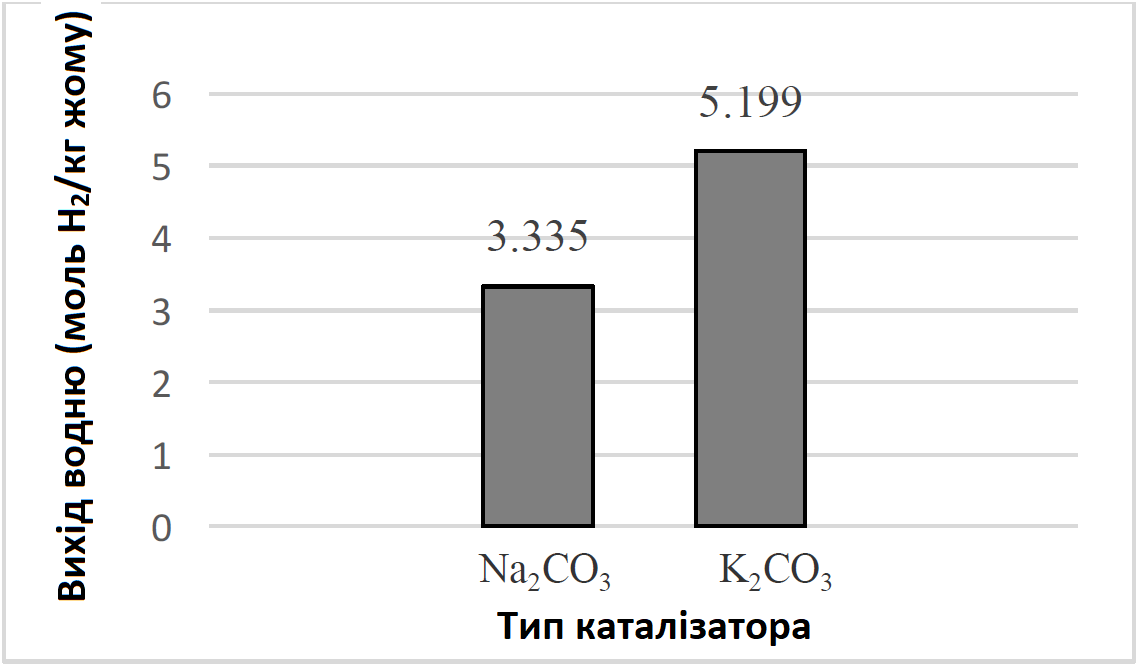
Для порівняння різної активності каталізатора K2CO3 проводилися подальші експериментальні дослідження з використанням 20% співвідношення кількості каталізатора до кількості сировини. Крім K2CO3, інший каталізатор на основі лугу Na2CO3 використовувався для дослідження різних характеристик каталізатора щодо виходу водню за відповідних умов, визначених для K2CO3. Порівняння активності каталізаторів K2CO3 і Na2CO3 у виробництві водню під час газифікації жому показано на Рис. 4.
Як показано на Рис. 4, незважаючи на те, що обидва каталізатори належать до однієї групи (періодичної таблиці), їх каталітична активність істотно відрізняється. Очевидно, що найбільший вихід Н2 з жому був досягнутий під час використання К2СО3. Зрештою, ефективність каталізатора Na2CO3 в контексті виходу водню під час газифікації жому була значно нижчою. Одним із можливих пояснень цього може бути коксоутворення, що призводить до дезактивації каталізатора. Іншим можливим поясненням є краща каталітична активність K лужного металу, порівняно з іншими. Згідно з оглядом літератури, за допомогою лужних каталізаторів газифікували різну біомасу, а також повідомлялося, що K2CO3 має кращий каталітичний ефект, ніж Na2CO3.
Рис. 4. Вплив типу каталізатора на вихід водню, отриманого під час газифікації жому (650°C, 20% співвідношення кількості каталізатора до кількості сировини, швидкість подачі повітря 2 л/год, час реакції 15 хв.)
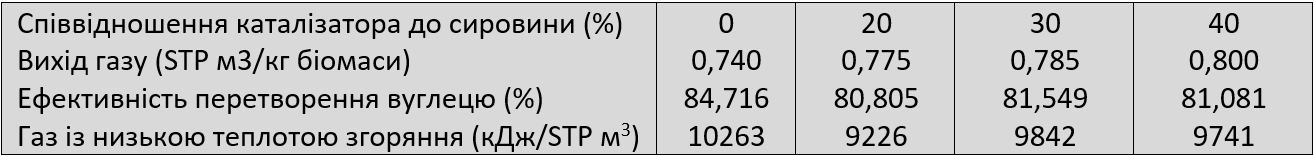
Каталітичні властивості K2CO3 щодо ефективності перетворення вуглецю та газу з низькою теплотою згоряння були досліджені при різному завантаженні каталізатора. Згідно з даними Таблиці 3, значне збільшення виходу газу не спостерігалося, коли коефіцієнт співвідношення кількості каталізатора до кількості сировини збільшувався з 20% до 40%. Однак, незалежно від цього, ефективність перетворення вуглецю залишалася практично незмінною. Крім того, найбільше значення газу з низькою теплотою згоряння було отримано за наявності 30% співвідношення кількості каталізатора до кількості сировини — 9 842 кДж/STP м3.
Таблиця 3. Експериментальний результат впливу різного співвідношення кількості каталізатора до кількості сировини (650°C, швидкість подачі повітря 2 л/год, час реакції 15 хв.)
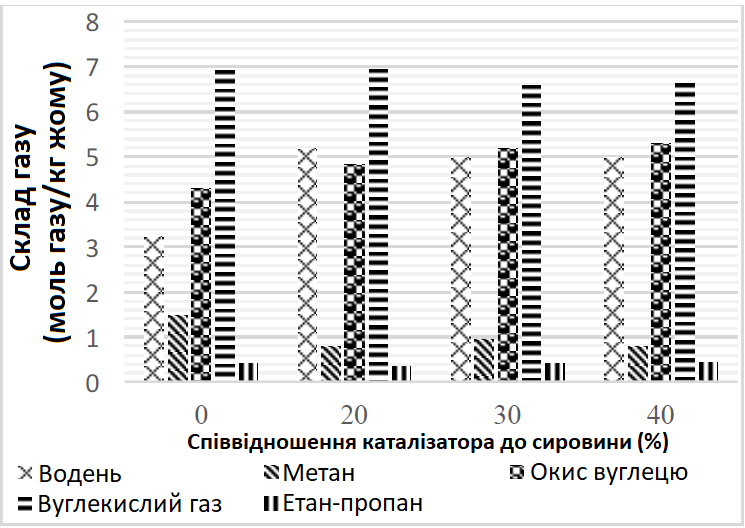
На Рис. 5 показаний газовий склад газифікації жому в залежності від різного коефіцієнту співвідношення кількості каталізатора до кількості сировини. Як зазначено вище, вміст водню значно збільшився з 3,220 до 5,199 моль H2/кг жому при 20% співвідношенні каталізатора до сировини. Однак подальше збільшення його відношення змінило селективність щодо Н2 і викликало зменшення. І навпаки, додавання каталізатора у співвідношенні 20% до сировини призвело до значного зниження вмісту CH4. Використання каталізатора сприяє реакціям крекінгу смоли, парового риформінгу та реакціям конверсії водяного газу. Отже, збільшення H2 і зменшення CH4 може бути зумовлено внеском цих реакцій. Крім того, CH4 продовжував демонструвати спадну тенденцію з додаванням каталізатора у співвідношенні 40% до сировини. На відміну від Н2 і СН4, вміст СО демонстрував протилежну тенденцію і постійно збільшувався під впливом різного коефіцієнту співвідношення каталізатора. Незважаючи на те, що за відсутності каталізатора та при 20% коефіцієнті співвідношення вміст СО2 залишався постійним, він досягнув максимального значення 6,640 моль газу/кг жому при 40% коефіцієнті співвідношення каталізатора до сировини. Вихід етан-пропану зменшився за рахунок збільшення коефіцієнту співвідношення каталізатора до 20%, а подальше збільшення цього коефіцієнту показало незначну зміну у виході етан-пропану. Результати порівняння впливу як температури, так і каталізатора на газифікацію жому показали, що температура мала більший вплив на склад продукту в межах діапазону, дослідженого в даній роботі. Таким чином, за допомогою збільшення температури було досягнуто більшого перетворення вуглецю, виходу газу та газу з низькою теплотою згоряння. Проте 20% коефіцієнт співвідношення кількості каталізатора K2CO3 до кількості сировини також показав значний вплив на збільшення виходу водню.
Рис. 5. Вплив коефіцієнту співвідношення кількості каталізатора до кількості сировини на склад газоподібного продукту (650°C, швидкість подачі повітря 2 л/год, час реакції 15 хв.)
Незважаючи на те, що переважає генераторний газ, під час процесу газифікації деяка частина біомаси розкладається на кокс та смолу. Відповідно до рішення, прийнятого на засіданні Європейського Союзу/Міжнародного енергетичного агентства/Департаменту енергетики США (EU/IEA/USA-DOE), термін «смола» визначається як усі органічні забруднювачі, молекулярна маса яких вища за бензол. Кокс — це твердий вуглець, що залишається після газифікації біомаси, який має високу теплотворну здатність. Відповідно мета процесу газифікації полягає в тому, щоб отримати максимальне газоутворення, яке може бути можливим шляхом видалення смоли та косового залишку. Однак реакції видалення смоли кінетично обмежені і включають температуру та/або каталізатор для прискорення швидкості реакції.
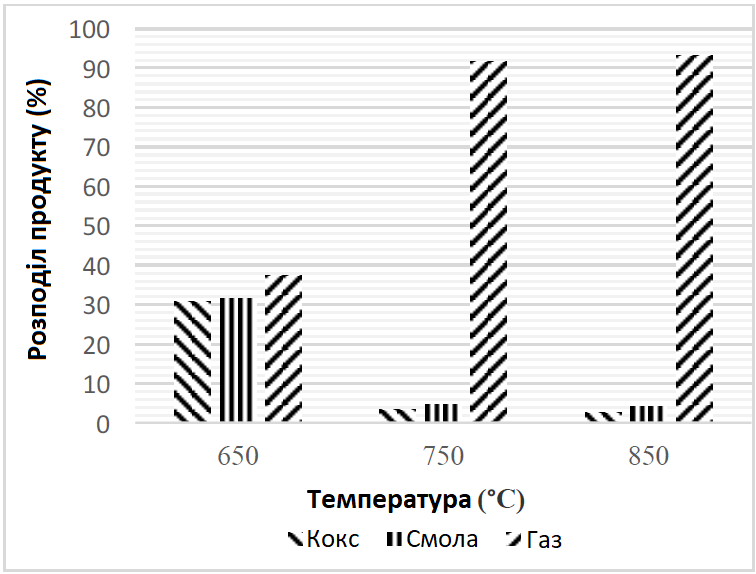
На Рис. 6 показано вплив температури на розподіл продукту газифікації (газу, смоли та коксу). Кількість смоли та коксу швидко зменшувалася з підвищенням температури з 650 °C до 750 °C, що викликало помітне збільшення виходу газу. У досліджуваному температурному діапазоні вихід коксу різко зменшився з 30,921 до 3,514%, тоді як вихід смоли знизився з 31,650 до 4,815%. Це вказує на те, що підвищення температури стимулювало такі процеси, як крекінг смоли та перетворення коксу. Вихід як смоли, так і коксу продовжував знижуватися з подальшим підвищенням температури і склав 2,542% і 4,283% при 850°C відповідно. Зменшення вмісту смоли та коксу призвело до відповідного збільшення виходу газу, який досягнув 93,180% при 850°C.
Рис. 6. Вплив температури на розподіл продукту (без каталізатора, швидкість подачі повітря 2 л/год, час реакції 15 хв.)
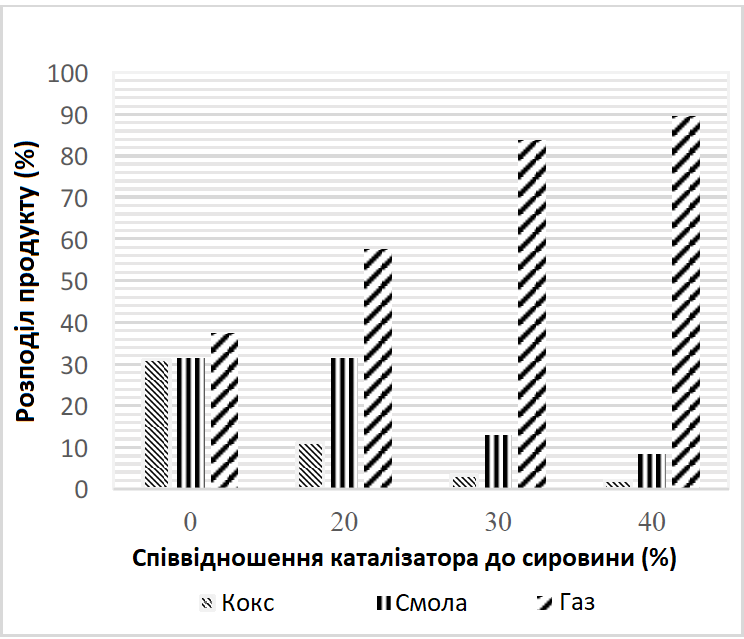
Зміну розподілу газового продукту із коефіцієнтом співвідношення каталізатора до сировини узагальнено на Рис. 7. Як показано, каталізатор демонстрував різну тенденцію до розподілу продукту, в порівнянні з температурою. Конверсія коксу поступово посилювалася подальшим додаванням каталізатора, і при 40% коефіцієнті співвідношення каталізатора до сировини залишалася невелика кількість коксу. Крім того, найвищий вихід смоли (31,473%) був отриманий за наявності 20% співвідношення каталізатора до сировини, який показав значне зниження при збільшенні співвідношення каталізатора до сировини від 20% до 40%. Однак разом із збільшенням співвідношення каталізатора до сировини вихід газу постійно зростав та досягнув максимального рівня 89,554% при 40% співвідношенні каталізатора до сировини. Порівнюючи випадки з каталізатором і без нього, можна помітити, що підвищення температури є відносно ефективнішим для мінімізації виходу смоли та коксу, отже, збільшення виходу газу.
Рис. 7. Вплив коефіцієнту співвідношення кількості каталізатора до кількості сировини на розподіл продукту (650°C, швидкість подачі повітря 2 л/год, час реакції 15 хв.)
Під час переробки цукрових буряків залишається не тільки жом, також відокремлюються відходи неекстрагованих цукрових буряків (WUNESB) та бадилля (гичка) перед тим, як цукровий буряк відправляється в систему екстракції. Усі ці відходи цукрової галузі створюють можливість для виробництва енергії, таким чином зменшуючи екологічні проблеми. Тому дане дослідження було розширено, щоб оцінити використання WUNESB, бадилля та їх суміші в якості вихідної сировини для виробництва водневмісного газу.
Відходи неекстрагованих цукрових буряків (WUNESB), бадилля та суміш відходів газифікували при 650°C, 20% K2CO3 та 15 хв. час реакції. Отримані результати (вихід водню) порівнювали з результатами жому (Рис. 8). Фізико-хімічний склад біомаси є важливим параметром для продуктивності процесу газифікації.
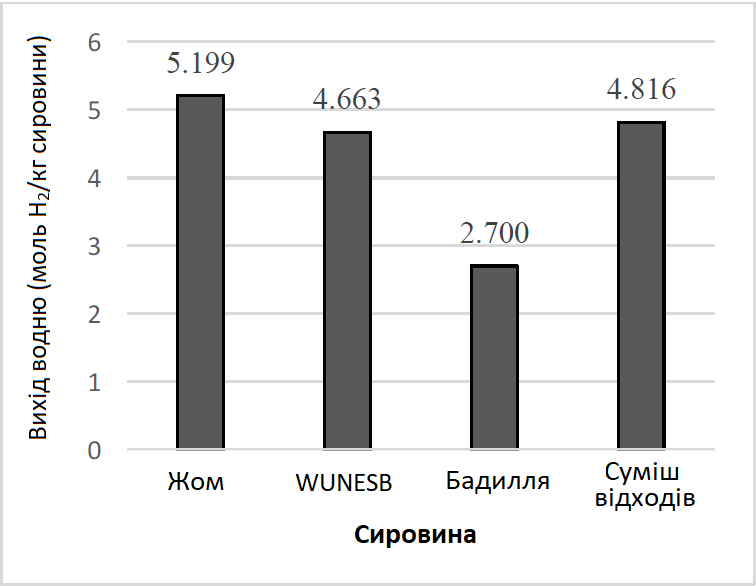
Целюлоза, геміцелюлоза та лігнін є основними компонентами біомаси. Крім того, вміст целюлози та геміцелюлози пов’язаний з виходом генераторного газу. Із Рис. 8 видно, що вихід водню із жому є відносно вищим, порівняно з іншими відходами цукрових буряків. Крім того, вихід водню з відходів неекстрагованих цукрових буряків (WUNESB) і суміші, яка містила рівну кількість відходів буряків, був дуже подібним і складав 4,663 моль H2/кг WUNESB і 4,816 моль H2/кг суміші, відповідно. Однак вихід водню з бадилля, з іншого боку, виявився незадовільним зі значенням 2,700 моль H2/кг бадилля. Це можна пояснити наступними причинами: менша частка вмісту целюлози та геміцелюлози та велика кількість екстрактивних речовин у бадиллі, які могли призвести до утворення смоли замість газоподібного продукту.
Рис. 8. Вихід водню з жому, відходів неекстрагованих цукрових буряків (WUNESB), бадилля та суміші відходів (650°C, 20% K2CO3, швидкість подачі повітря 2 л/год, час реакції 15 хв.)
Висновки
Серед відновлюваних джерел енергії біомаса привертає до себе все більше уваги через різноманітність сировини та способів використання відходів. Метою даної роботи є дослідження потенціалу жому, який є побічним продуктом цукрового заводу, як альтернативи традиційним джерелам енергії з використанням технологій газифікації. Під час виробництва генераторного газу в якості окислювача використовувалося сухе повітря. Експерименти з газифікації проводилися з використанням різних робочих параметрів, включаючи різну температуру (650°C, 750°C та 850°C), без каталізатора та з лужними каталізаторами (K2CO3, Na2CO3). Генераторний газ, утворений в процесі газифікації, був ідентифікований за допомогою системи мікрогазової хроматографії. З отриманих результатів встановлено, що найвищий вихід водню становить 5,730 моль H2/кг біомаси за відсутності каталізатора при 850°C зі швидкістю подачі повітря 2 л/год і 15 хв. час реакції. Крім того, було виявлено, що каталізатор K2CO3 більш ефективний, ніж Na2CO3, а максимальний вихід водню (5,199 моль H2/кг біомаси) був досягнутий при використанні K2CO3 при 650°C із швидкістю подачі повітря 2 л/год і 15 хв. час реакції.
Виробництво генераторного газу шляхом газифікації біомаси може стати альтернативою для зменшення залежності від викопного палива. Дане дослідження було зосереджено на процесі газифікації відходів цукрових буряків у трубчастому газогенераторі висхідного потоку з використанням повітря як газифікуючого агента для отримання водневмісного газу. Проаналізовано вплив експериментальних параметрів на вихід та склад газу, ефективність конверсії вуглецю, газу з низькою теплотою згоряння.
Температура виявилася найважливішим впливовим фактором газифікації жому.
При підвищенні температури реакції від 650 до 850°C вихід водню постійно збільшувався, показник приросту досягнув 78% без використання каталізатора. Крім того, вища температура призвела до більшого виходу газу — 0,900 STP м3/кг жому, досягнутого при 850°C. Тенденція ефективності конверсії вуглецю при газифікації жому подібна до виходу газу, максимальне значення було отримано при 850°C — 95,061%. Підвищення температури не завжди позитивно впливало на газ із низькою теплотою згорання, оскільки при 750°C його вихід був меншим, ніж при 650°C, тоді як найвище значення газу з низькою теплотою згорання (10298 кДж/STP м3) було зафіксовано при 850 °C.
За каталітичних умов найвищий вихід водню (5,199 моль H2/кг жому) був досягнутий при 20% співвідношенні каталізатора (K2CO3) до сировини. Крім того, були досліджені різні каталітичні впливи на вихід водню під час газифікації жому, було виявлено, що тип каталізатора мав помітний вплив на вихід водню. За тих же умов роботи каталізатор Na2CO3 виявляв нижчі рівні активності щодо виробництва водню. З іншого боку, вихід газу продовжував зростати з невеликим приростом у міру збільшення співвідношення каталізатора до сировини, а найвищий вихід газу досягнув 0,800 STP м3/кг жому. Крім того, найвища ефективність перетворення вуглецю (81,549%) та вихід газу з низькою теплотою згорання (9842 кДж/STP м3) були отримані при 30% співвідношенні каталізатора K2CO3 до сировини.
Суміш, яка містила однакову кількість жому, відходів неекстрагованих цукрових буряків (WUNESB) і бадилля, використовувалася для визначення виходу водню, було виявлено, що при 650°C вихід водню склав 4,816 моль H2/кг суміші з 20% K2CO3, що подібно до результатів, отриманих за тих же умов під час газифікації жому. Це означає, що всі відходи цукрового заводу можна використовувати безпосередньо в суміші, тобто без розділення.